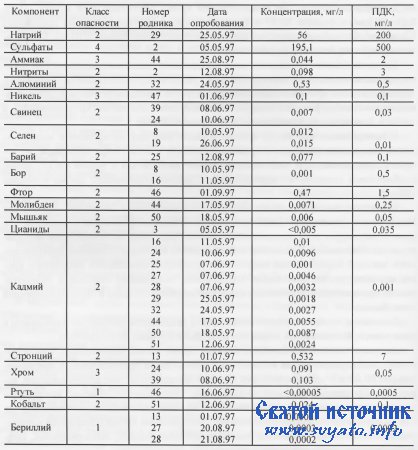
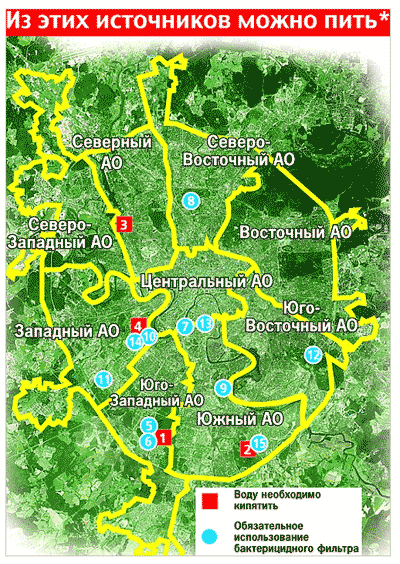
Основные компоненты-загрязнители родниковых вод МосквыАвтор: Плаксин ОлегОпубликовано: 4 апреля 2013 г. 12:55, посмотрело: 5852 Москва Характеристика наиболее опасных компонентов - загрязнителей, обнаруженных в воде исследуемых Московских родников.
Селен (Se) Загрязнение родниковых вод селеном отмечено в родниках музея-заповедника Коломенское (родники № 2, 8) - на уровне 0,01-0,03 мг/дм3 (при ПДК = 0,01 мг/дм3) и на уровне 0,02 мг/дм3 в районе Царицынских прудов. Участки загрязнения территориально близки, входят в один административный район, что косвенно свидетельствует об общих источниках загрязнения грунтовых вод. Такими природными источниками могут быть породы и почвы, а также горнодобывающие производства и инженерно-хозяйственная деятельность человека. Селен относится к очень редким летучим элементам, обладающим одновременно неметаллическими и полуметаллическими свойствами, повышенной биофильностью и высокой токсичностью. ПДК в водах хозяйственно-питьевого назначения - 0,01 мг/дм3. Если рассматривать в качестве возможного источника появления Se в подземных водах горные породы, то следует сказать, что всего известно до 70 минералов-селенитов. Наиболее типичны медные и никелевые (более половины), а из наиболее часто встречающихся известен клаусталит (PbSe). Иногда относительно широко распространены самородный селен (Se), кадмоселит (CdSe), ферроселит (FeSe), селениды меди. Все минералы относятся к числу редких и весьма редких и могут быть пропущены при минералогических исследованиях. В промышленных типах месторождений Se встречается в виде примесей в халькопирите, галените, пирите, сфалерите. Изучение распределения Se в почвах имеет важное значение, так как повышенные его концентрации могут вызвать тяжелые заболевания. Иногда в почвах на черных сланцах содержание Se увеличивается до 1-4 г/т. Низкие содержания Se (+200 мВ), приуроченные к областям питания водоносных горизонтов и имеющие сульфатный состав, содержат селенаты, селениты, гидроселениты и органические соединения Se. В них концентрация Se достигает п-10 мкг/ дм3. 5. Воды с низкими значениями Eh (-200-+100 мВ), формирующиеся в погруженных частях артезианских бассейнов, имеют повышенную минерализацию и HC03-Na или HC03-S04-Na состав. Концентрация Se здесь тоже достаточно высока, но не более 1 мкг/дм3. Большое влияние на мобилизацию Se и его массоперенос оказывает растворенное органическое вещество. Его наличие увеличивает содержание Se до 5 мкг/дм3. Техно- и экогеохимия селена изучены недостаточно. Общие выводы, к которым мы пришли при анализе литературы, формулируются следующим образом: 1. Значительное количество селена поступает в окружающую среду при добыче и обогащении руд, так как Se легко летучий компонент и его потери достигают 50-90%. 2. Основными загрязнителями окружающей среды этим элементом являются селеновые, серные, медные, никелевые, фосфатные производства, тепловые электростанции, предприятия органического синтеза, фотоматериалов, полупроводников, электроники, керамики, эмалей, резинотехнических изделий, типографских красок, смазочных масел и др. Кадмий (Cd) Это редкий элемент, его кларк - 0,000016%, он сильно токсичен, обладает канцерогенными свойствами. ПДК в водах хозяйственно-питьевого назначения - 0,001 мг/дм3. Загрязнение родниковых вод кадмием имеет для Москвы региональный характер. Его содержание отмечено в водах родников, расположенных в Коломенском, Царицыно, Битцевском лесопарке, Теплом Стане, Ясенево, на Воробьевых горах и Крылатских холмах, в Филевском лесопарке, Свиблово и в Нескучном саду. Концентрации кадмия колеблются в диапазоне от 0,001 до 0,1 мг/дм3 и достигают максимума в одном из родников на Воробьевых горах (№ 44 - Ccd= =0,0055 мг/дм3) и в роднике Свиблово (№ 50 - Ccd= 0,0087 мг/ дм3). Источником поступления кадмия в подземные воды могут быть примеси в минералах, в основном в сульфидах. Чаще других встречаются сульфид-гринокит (CdS), селенид-кадмоселит (CdSe) и карбонаты кадмия. Согласно В.В. Иванову, повышенные содержания кадмия характерны для таких сульфидов, как сфалерит, станнин, халькопирит. Важно отметить геохимическое сродство кадмия и селена: они образуют общий минерал (кадмоселит - CdSe), а также часто встречаются в виде примесей в одних и тех же сульфидах - сфалерите и халькопирите. Почво- и биогеохимия кадмия в связи с его высокой токсичностью изучены довольно полно. В зоне гипергенеза он легко переходит в раствор в виде ионов Cd2+ и комплексов CdCl+, CdOH+, CdHC03+ и др. В кислых почвенных растворах кадмий присутствует в форме Cd2+, CdCl+, CdS04. По данным экологов ЕС, к 1970 г. содержание кадмия в почвах превысило многолетнюю норму (=0,1 мг/кг). При этом прогноз предполагает, что увеличение концентраций кадмия будет продолжаться с интенсивностью 0,1 мг/кг почвы каждые 20-30 лет. Например, для бывшей ФРГ загрязнение,окружающей среды кадмием за один год происходит за счет: 1) осаждения из воздуха =3-5 г/га; 2) с биологическим илом =1 г/га; 3) с фосфорными удобрениями =5-6 г/га; 4) из других источников - до 1 г/га. Концентрации кадмия в почвах около промышленных предприятий (в мг/кг) составляют: радиотехническое производство - 400; сжигание мусора - 170; производство сплавов - 100; цветных металлов - 80; лакокрасок - 12. Биологически полезного воздействия кадмия на растения не отмечалось, тогда как признаки угнетения ячменя на дерново-подзолистых почвах появлялись уже при внесении кадмия в количестве 10 мг/кг. Несмотря на токсичность кадмия для человека, его биологическая роль до конца не выяснена. Так, по данным Д. Эмсли, он является стимулятором и канцерогеном. Отрицательное действие больших доз кадмия может отразиться на таких органах как легкие, простата, семенники, сердце, сосудистая система. В водах поверхностных водотоков концентрации кадмия составляют 0,1- 2 мкг/дм3. В подземных водах зоны гипергенеза среднее содержание кадмия составляет 3,3-10^ мг/дм3. Согласно Г.А. Голевой, концентрация кадмия в кислых водах зоны окисления рудных месторождений достигает 20 мг/дм3. По А.И. Перельману, кадмий относится к высокоподвижным элементам кислых вод зоны гипергенеза. С этим связана его высокая миграционная способность в кислых средах, а в щелочных наоборот, низкая, что приводит к его накоплению в зонах окисления сульфидных руд в карбонатных породах. Накопление кадмия характерно также для высокоминерализованных подземных вод. Техногенное воздействие кадмия особенно велико в связи с его способностью к накоплению во времени. В свое время (1979 г.) правительство Швеции приняло решение о запрещении не только производства и импорта, но и применения кадмийсодержащих продуктов. По данным Б.А. Ревича, Ю.Е. Саета и PC. Смирновой, кадмий в наибольшей степени накапливается в отходах гальванотехники, в радиотехническом и лекарственном производствах, при сжигании бытового мусора. По Я.М. Грушко, основными загрязнителями окружающей среды и родниковых вод в том числе являются производства: металлургические (особенно Pb-Zn-Cd), металлических покрытий, аккумуляторные, красильные, резиновые, пластмассовые, фосфорные, фотоматериалов, химической промышленности, мыловаренные, текстильные. Сопоставляя источники загрязнения Cd и Se, мы можем найти много общего. Работами Б.А. Колотова, В.З. Рубейкина, Е.А. Киселевой было изучено распределение кадмия вблизи шоссе Москва-Владимир и показано, что ширина полосы загрязнения по обе стороны от шоссе составляет 7-30 м. Для Москвы особая загрязненность окружающей среды кадмием отмечена для МКАД и особенно для района Капотни. Барий (Ва) Загрязнения родниковых вод г. Москвы барием за период ведения режимных наблюдений за их качеством не наблюдалось, но замечено, что концентрации бария в родниковых водах приближаются к ПДК (0,1 мг/ дм3) для родников в Теплом Стане (№ 25), в Ясенево (№ 28), в Филях (№ 32) и в Свиблово (№ 50). То есть регионального загрязнения родниковых вод этим компонентом не отмечается, но некоторое превышение фона, приближающееся по концентрации к ПДК, отмечено в виде локальных участков на Юго-Западе, Юге и Северо-Востоке Москвы. Барий - распространенный элемент, его кларк 0,047%. Он сильно токсичен. Минералы бария многочисленны (до 102 минералов), но в подавляющем большинстве встречаются редко. Рассматривать породы как источники загрязнения грунтовых вод барием вряд ли целесообразно. По данным П.Г. Адерихина и К.И. Лукашева, содержание бария в различных типах почв нашей страны колеблется в широких пределах (мкг/кг): от 80-100 в органических почвах до 600-900 в черноземах и лесных почвах. В аридных условиях в корках на поверхности почв количество бария увеличивается. Для растений токсичность бария не изучена. Для наземных животных его токсичность ощутимо высока. Пороговая концентрация в воде (мг/дм3), не влияющая на санитарный режим, - 10 мг/дм3; 50 мг/дм3 ВаСЦ вызывает отравление, а 150 мг/дм3 - гибель лососевых рыб. Для человека соединения бария высоко токсичны. Смертельная доза ВаС12 - 0.8-0.9 г/дм3, ВаСО, - 2-4 г/дм3. Содержания бария в подземных водах зоны гипергенеза, по А.И. Перельману, зависят от ландшафтно-климатических условий и составляют (мкг/дм3): области континентального засоления - 50,1; зоны выщелачивания - 12,0; области умеренного климата - 16,7; горные районы - 14,1; мерзлотные области - 9,5; субтропики - 7,8. Для накопления бария предпочтительнее хлоридные и гидрокарбонатные воды. Техногеохимия бария изучена недостаточно хорошо. На бариевых производствах прежде всего опасна пыль, а также сточные и технические воды. Установлен барий в пыли некоторых производств: коксохимического, механического (литейные производства, обработки чугуна), цементного (мельницы, цеха обжига), а также при производстве вторичного алюминия. Кроме того, барий содержится в выбросах тех же самых производств, которые опасны с позиции загрязнения Cd и Se. Дополнительно опасными являются деревообрабатывающая, пищевая (сахар, жиры), кожевенная, фармацевтическая отрасли промышленности, производство иодидов, бромидов, серной кислоты, пестицидов и др. Бериллий (Be) Концентрации бериллия, близкие по величине к ПДК (0,0002 мг/дм3), определены в водах 3-х родников: в Коломенском (в тыловом шве поймы р. Москвы - родник №13) и в Битцевском лесопарке (родники № 27, 28). Бериллий - редкий элемент, его кларк 0,0002%, легкий, высоко токсичный и канцерогенный, биологически активный металл. Известно 62 бериллиевых минерала. Это в основном силикаты: берилл, фенакит, эпидидимит, лейкофан, бехоит, бертрандит, гельвин, барилит и др. Главные минералы бериллия образуют следующий ряд по снижению степени их устойчивости в коре выветривания: берилл (1,3), эпидидимит (0,98), бертрандит (0,6), фенакит (0,575), гаролинит (0,335). Берилл, хотя и считается устойчивым минералом, но в ассоциации с флюоритом подвержен изменению с формированием гипергенных фосфатов. При выветривании породообразующих минералов-носителей Be наиболее интенсивно выносится при разложении мусковита и иногда калиевого полевого шпата. В осадочных породах максимальные концентрации бериллия характерны для глин (до 11 г/т), в песчаных и карбонатных породах они ниже - 8 и 5,5 соответственно. В незагрязненных почвах средние концентрации бериллия колеблются от 1 до 15 мг/кг. Бериллий токсичен для растений, так как тормозит прорастание семян и потребление Са, Mg, Р, разрушает протеины. Отмечается, что повышенные концентрации бериллия в окружающей среде могут вызывать раковые заболевания у человека и, по данным НИИканцерогенеза онкоцентра РАМН, принятые ПДК для бериллия не обеспечивают полной безопасности. Гипергенное преобразование бериллийсодержащих минералов приводит к обогащению бериллием подземных вод, взаимодействующих с этими минералами. Хотя совсем недавно считалось, что бериллий практически не мигрирует в подземных водах, он образует подвижные комплексы с F", что особенно важно для зоны гипергенеза в Москве и области, в пределах которых отмечаются повышенные концентрации F и тогда бериллий активно мигрирует в грунтовых водах с образованием отрицательных фторкомплексов:ВеР3~, BeF42 . Отмечено, что бериллийсодержащие воды не пригодны для питья, особенно в гумидных районах развития кислых-щелочных интрузивно-эффузивных пород с повышенными концентрациями Be и F, в районах с редкометальной сульфидной минерализацией. Поскольку таких условий на территории Москвы и области нет, то причину повышенных концентраций бериллия в грунтовых родниковых водах следует искать в их техногенном загрязнении. Изучены только условия, связанные с загрязнением окружающей среды бериллием в связи с бериллиевым производством. Особенно опасны аварийные ситуации (загорание и взрывы бериллиевой пыли на Ульбинском металлургическом заводе обеспечили превышение ПДК бериллия в атмосфере в 60-900 раз, последствия аварии не предсказуемы). Повышенные концентрации бериллия обнаружены при производстве сплавов в цветной металлургии, пластмасс, огнеупоров, в машиностроении, на предприятиях стройматериалов. Известны превышения ПДК по бериллию в сбросах электро- и радиотехнического приборостроения, ядерной энергетики, ракето- и самолетостроения, в сточных промышленных водах, используемых для орошения. Марганец (Мп) В количествах, превышающих или близких к ПДК (0,1 мг/дм3), марганец обнаружен в 3-х родниках Москвы. Концентрации марганца в роднике № 50 в Свиблово и № 51 в Нескучном саду приближаются к ПДК и составляют 0,05- 0,07 мг/дм3, а в роднике № 60, расположенном в долине р. Сетуни (дер. Чоботы), отмечено двойное превышение ПДК по марганцу. Марганец является широко распространенным элементом, его кларк 0,09%. Это жизненно необходимый, но токсичный металл. Минералогия марганца разнообразна и известно до 110 силикатов, 47 фосфатов, 32 оксида, 27 гидроксидов, 29 арсенатов и т.д. Одно то, что марганец способен к гипергенному минерал ооб^зрванию (фосфаты, оксиды, гидроксиды) говорит о том, что породы могут быть реальным источником его накопления в подземных водах. Вместе с тем, из осадочных образований наиболее обогащены марганцем глубоководные фации (глины - до 0,7%, карбонаты - до 0,2%). В почвах марганец распространен широко и играет большую роль в формировании их химического состава. Среднее содержание марганца в почвах 850мг/кг. Отмечается двойное влияние марганца на живые организмы и растения. Недостаток и избыток марганца ведет к возникновению заболеваний или прогрессу патологий. Максимальными концентрациями Мп в почвах характеризуются таежные, лесостепные и степные черноземные ландшафты, где доля марганца составляет от 0,5 до 12%. Отмечено, что недостаток марганца в почвах (30%) приводит к токсичному влиянию всех групп растений, особенно на кислых почвах. Регулируется количество марганца в почвах введением удобрений MnS04-5H20 (он входит в суперфосфат, аммофос) и в некоторых случаях они же служат очагами загрязнения почв и подземных вод. Для человека марганец токсичный и в то же время совершенно необходимый элемент. Он обладает антиканцерогенными свойствами, оказывает положительное влияние на ферментные системы мозга. Избыток Мп приводит к необратимым нарушениям центральной нервной системы. В водах рек марганец обычно имеет концентрации 0,015-0,25 мг/дм3. На гидропостах, расположенных ниже городов, они возрастают до 0,07-0,4 мг/дм3. Но сам Мп концентрируется в илах (до 300-600 мг/дм3). В воде мигрирует в основном в неорганических формах (ионы, молекулы, неорганические комплексы). В подземных водах максимально известное содержание Мп достигает 2000 мг/дм3. К геохимическим типам Mn-содержащих вод среди подземных вод, используемых для питьевого водоснабжения, относятся два основных: 1) с высоким содержанием органики; 2) бескислородно-бессульфатные пластовые воды. И тот, и другой одновременно содержат повышенные концентрации Fe2+, Fe3+, что в общем хорошо согласуется с данными по родникам № 50, 51 и 60. Концентрации Fe2+, Fe3+ в их водах достигают 5-12 мг/дм3 (при ПДК 0,3 мг/дм3). Главным источником поступления избыточного марганца в окружающую среду является горнодобывающая и горнообогатительная промышленность. Дополнительно марганец поступает в атмосферу, почвы, грунтовые воды в виде отходов цветной металлургии (производство вторичного алюминия), чугуно-литейной, машиностроительной и металлообрабатывающей промышленности (в больших дозах до п-10 мг/дм3). Избыток марганца придает питьевой воде неприятный вкус и цвет (при концентрациях >0,15 мг/дм3). Хром (Сг) Хром встречен в 2-х родниках на территории Москвы. Это родник Бекет на Загородном шоссе, где концентрация хрома достигает 0,09 мг/дм3 (ПДК 0,05 мг/ дм3) и родник № 39 в Тропареве, где концентрация хрома составляет 0,1 мг/дм3. Он избирательно, но широко распространен (кларк 0,01%), биологически слабо изучен, сильно токсичен. Единственными промышленными минералами являются представители группы хромшпинелидов (изоморфный ряд хромиты-хромшпинелиды-шпинели). Технофильность хрома высокая. Он используется в металлургической, огнеупорной, стекольной отраслях в виде сплавов, порошков покрытия (хромирование), а также в текстильном, кожевенном и др. производствах. В гипергенных процессах хромит и некоторые другие хромовые минералы устойчивы к выветриванию и хром присутствует в остаточном материале, из которого при длительном окислении он может выноситься в форме СЮ42~, слабо сорбируемой глинами и гидроксидами. Среднее содержание хрома в почвах 100 г/т. Биологическое значение хрома изучено недостаточно. Известно, что он, как Mn, F, Se и др., оказывает двойное действие на живые организмы. Считается, что хром стимулирует рост сельскохозяйственных растений, но его избыток вызывает у них заболевания. У человека избыток хрома вызывает снижение толерантности к глюкозе, ослабленный метаболизм углеводов, повышение инсулина в крови, задержку роста, повышение холестерина, повышение опасности склеротических проявлений, снижение деятельности нервной системы и оплодотворяющей способности. Считается, что в поверхностных водах (в реках) хром мигрирует в основном в виде взвеси. В подземных водах его поведение изучено недостаточно. Антропогенное и техногенное влияние хрома весьма значительно. Самая высокая концентрация хрома в производственной пыли промышленных предприятий (пТОО мг/м3) установлена для цветной металлургии, металлообработки, керамической промышленности и гальваники. Затем идут (п-10 мг/м3) инструментальное производство, сжигание бытового мусора, производство алюминия и т.д. Среди других производств наиболее часто соединения хрома содержатся в отраслях каталитических процессов, текстильных, кожевенных, лакокрасочных, нефтехимических, стекольных производств. В заключение краткого анализа геохимических особенностей некоторых элементов-загрязнителей подземных вод необходимо добавить следующее. К наиболее распространенным токсичным веществам, по данным медицины, относятся: бензин, дихлорэтан, азотная, серная, соляная, уксусная и щавелевая кислоты, нитриты, окись углерода, сероводород, барий, йод, литий, медь, мышьяк, ртуть, таллий, цианиды, четыреххлористый углерод, хлор, хлорорганические соединения и др. Это далеко не весь список ядовитых веществ, способных оказывать вредное влияние на растения, животных и человека. В ходе наших исследований родниковых вод определялись следующие компоненты: барий, хлориды, медь, мышьяк, нитриты, ртуть и цианиды, натрий, сульфаты, аммиак, алюминий, никель, свинец, селен, бор, фтор, молибден, кадмий, стронций, хром, кобальт, бериллий. Диапазон их класса опасности охватывает все ранги градации, то есть среди вышеперечисленных компонентов есть как наименее опасные, относимые к 4 классу, так и чрезвычайно опасные, относящиеся к 1 классу опасности. В таблице указаны изученные химические элементы, ПДК которых устанавливается по токсикологическому признаку вредности. Из таблицы следует, что элементы, превышающие установленные нормы их содержания в водах хозяйственно-питьевого назначения, принадлежат в основном ко 2-му классу опасности. Вещества этого класса при превышении их концентрации относительно ПДК в 3-10 раз могут привести к появлению у населения симптомов интоксикации и развитию отдельных негативных эффектов. Воды с таким уровнем содержания токсичных элементов имеют высокую степень загрязнения и представляют безусловную опасность при их использовании в питьевых целях. Подводя итог изучению химического состава родниковых вод в период 1997- 2001 гг., можно сделать следующие выводы: - отмечается определенное совпадение пиков концентраций отдельных компонентов-загрязнителей с периодами половодья и паводка р. Москвы и ее притоков; - нерегулярность превышения ПДК компонентами-загрязнителями по времени указывает на техногенный источник их поступления в подземные воды; - замечена довольно четкая противофазная зависимость изменения концентраций железа и фтора, которая может в результате проведения глубокого гидрогеохимического анализа объяснить наличие весьма заметной отрицательной геохимической аномалии фтора грунтовых вод; - концентрационный уровень содержания большинства компонентов-загрязнителей в 2000 году несколько выше, чем в 1997 г. (по августу месяцу), при этом в 2000 году вещества находятся в пределах ПДК. Статья составлена по данным фундаментальной сводки В.В. Иванова [1996]. Источник "Родники Москвы" Научный мир, Москва, 2002 г. Коллектив авторов Владимира Михайловича Швеца Александра Борисовича Лисенкова Евгения Владимировича Попова
| ||